- Автор Alex Aldridge aldridge@what-difference.com.
- Public 2023-12-17 13:44.
- Акыркы өзгөртүү 2025-06-01 07:37.
Негизги айырма - Күчтүү Лиганд менен Алсыз Лиганд
Лиганд - бул борбордук атом же ион менен координаталык коваленттик байланыш аркылуу өзүнүн эки электронун берген же бөлүшкөн атом, ион же молекула. Лиганддардын түшүнүгү координациялык химиянын алкагында талкууланат. Лигандалар - металл иондору менен комплекстерди түзүүгө катышкан химиялык түрлөр. Демек, алар комплекстүү агенттер катары да белгилүү. Лигандалар лиганддын тиштүүлүгүнө жараша моноденттүү, экидентүү, үч тиштүү ж.б. Тиштүүлүк - бул лиганддагы донордук топтордун саны. Monodentate лиганда бир гана донордук топ бар экенин билдирет. Bidentate анын бир лиганд молекуласына эки донордук тобу бар дегенди билдирет. Кристалл талаасынын теориясынын негизинде классификацияланган лиганддардын эки негизги түрү бар; күчтүү лиганддар (же күчтүү талаа лиганддары) жана алсыз лиганддар (же алсыз талаа лиганддары). Күчтүү лиганддар менен алсыз лиганддардын ортосундагы негизги айырма, күчтүү талаа лигандына туташкандан кийин орбиталдардын бөлүнүшү жогорку жана төмөнкү энергетикалык деңгээлдеги орбиталдардын ортосунда чоң айырмачылыкты жаратат, ал эми алсыз талаа лигандына байланышкандан кийин орбиталдардын бөлүнүшү азыраак айырмачылыкты жаратат. жогорку жана төмөнкү энергетикалык деңгээлдеги орбиталдардын ортосунда.
Кристалл талаасынын теориясы деген эмне?
Кристаллдардын талаасынын теориясын айланадагы статикалык электр талаасынан улам электрондук орбитальдардын (көбүнчө d же f орбиталдарынын) бузулушунун (тең энергиядагы электрон кабыктары) бузулушун түшүндүрүү үчүн иштелип чыккан модель катары сүрөттөлсө болот. анион же аниондор (же лиганддар). Бул теория көбүнчө өтмө металл иондор комплекстеринин жүрүм-турумун көрсөтүү үчүн колдонулат. Бул теория магниттик касиеттерин, координация комплекстеринин түстөрүн, гидратация энтальпияларын ж.б. түшүндүрө алат.
Теория:
Металл иону менен лиганддардын өз ара аракеттешүүсү оң заряддуу металл ионунун жана лиганддын жупташпаган электрондорунун терс зарядынын ортосундагы тартылуунун натыйжасы. Бул теория негизинен беш бузулган электрон орбиталында (металл атомунун беш d орбиталында) болгон өзгөрүүлөргө негизделген. Лиганд металл ионуна жакындаганда жупташкан электрондор металл ионунун башка d орбиталдарына караганда кээ бир d орбиталдарына жакыныраак болот. Бул дегенерация жоготууга алып келет. Жана ошондой эле d орбитальдардагы электрондор лиганддын электрондорун түртүшөт (анткени экөө тең терс заряддуу). Демек, лигандага жакын турган d орбиталдары башка d орбиталдарына караганда жогорку энергияга ээ. Бул энергиянын негизинде d орбиталдарынын жогорку энергиялуу d орбиталдарына жана аз энергиялуу d орбиталдарына бөлүнүшүнө алып келет.
Бул бөлүнүүгө таасир эткен кээ бир факторлор; металл ионунун табияты, металл ионунун кычкылдануу даражасы, борбордук металл ионунун айланасында лиганддардын жайгашуусу жана лиганддардын табияты. Бул d орбитальдар энергиянын негизинде бөлүнгөндөн кийин, жогорку жана төмөнкү энергиялуу d орбиталдарынын ортосундагы айырма кристаллдык талаанын бөлүнүү параметри катары белгилүү (∆oct октаэдрдик комплекстер үчүн).
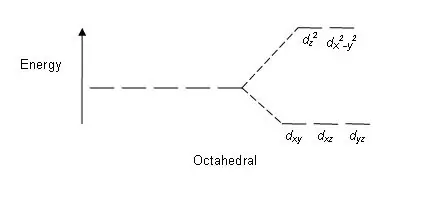
01-сүрөт: Октаэдрдик комплекстердеги бөлүү үлгүсү
Бөлүү үлгүсү: Беш d орбитал бар болгондуктан, бөлүнүү 2:3 катышында болот. Октаэдрдик комплекстерде эки орбитал жогорку энергия деңгээлинде (жалпысынан "мис" деп аталат), үч орбитал төмөнкү энергетикалык деңгээлде (жалпы t2g деп аталат) болот. Тетраэдрдик комплекстерде тескерисинче болот; үч орбитал жогорку энергетикалык деңгээлде жана экөө төмөнкү энергетикалык деңгээлде.
Стронг Лиганд деген эмне?
Күчтүү лиганд же күчтүү талаа лиганды кристалл талаасынын жогорку бөлүнүшүнө алып келе турган лиганд болуп саналат. Бул күчтүү талаа лигандынын байланышы жогорку жана төмөнкү энергетикалык деңгээлдеги орбиталдардын ортосунда чоң айырмачылыкты пайда кылат дегенди билдирет. Мисалдарга CN- (цианиддик лиганддар), NO2- (нитролиганд) жана CO (карбонил) кирет лиганддар).
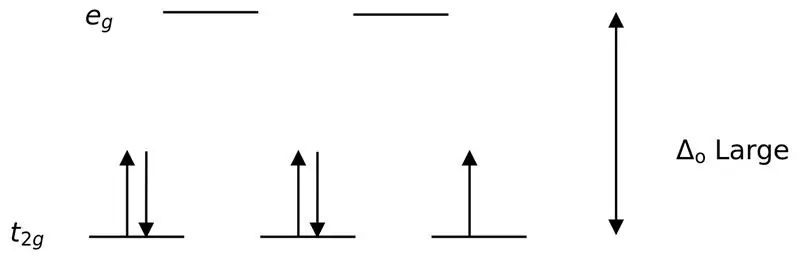
02-сүрөт: Айлануунун аз бөлүнүшү
Бул лиганддар менен комплекстерди пайда кылууда адегенде төмөнкү энергетикалык орбитальдар (t2g) башка жогорку энергетикалык деӊгээлдеги орбитальдарга (мисалы) толордон мурун толугу менен электрондор менен толтурулат. Ушундай жол менен түзүлгөн комплекстер "төмөн айлануучу комплекстер" деп аталат.
Алсыз лига деген эмне?
Алсыз лиганд же алсыз талаа лигандасы төмөнкү кристалл талаасынын бөлүнүшүнө алып келе турган лиганд болуп саналат. Бул алсыз талаа лигандынын байланышы жогорку жана төмөнкү энергетикалык деңгээлдеги орбитальдардын ортосундагы айырманы азыраак жаратат дегенди билдирет.
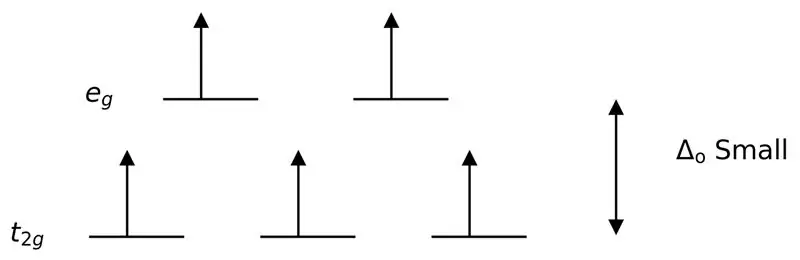
3-сүрөт: Жогорку айлануу менен бөлүнүү
Мында, эки орбиталык деңгээлдин ортосундагы аз айырма ошол энергетикалык деңгээлдердеги электрондордун ортосунда түртүүнү пайда кылгандыктан, аз энергиялуу орбитальдарга салыштырмалуу жогору энергиялуу орбитальдарды электрондор оңой толтурса болот. Бул лиганддар менен түзүлгөн комплекстер "жогорку спиндик комплекстер" деп аталат. Алсыз талаа лиганддарынын мисалдарына I- (иодид лиганд), Br- (бромдук лиганд) ж.б. кирет.
Күчтүү лиганд менен алсыз лиганддын ортосунда кандай айырма бар?
Күчтүү Лиганд vs Алсыз Лиганд |
|
| Күчтүү лиганд же күчтүү талаа лиганды - бул кристалл талаасынын көбүрөөк бөлүнүшүнө алып келиши мүмкүн болгон лиганд. | Алсыз лиганд же алсыз талаа лиганды - бул лиганд, ал төмөнкү кристалл талаасынын бөлүнүшүнө алып келиши мүмкүн. |
| Теория | |
| Күчтүү талаа лигандын байланыштыргандан кийин бөлүнүү жогорку жана төмөнкү энергетикалык деңгээлдеги орбитальдардын ортосундагы чоң айырманы пайда кылат. | Алсыз талаа лигандын байлагандан кийин орбиталдардын бөлүнүшү жогорку жана төмөнкү энергетикалык деңгээлдеги орбитальдардын ортосундагы айырманы азыраак жаратат. |
| Категория | |
| Күчтүү талаа лиганддары менен түзүлгөн комплекстер "төмөн спиндик комплекстер" деп аталат. | Алсыз талаа лиганддары менен түзүлгөн комплекстер "жогорку спиндик комплекстер" деп аталат. |
Кыскача - Күчтүү Лиганд менен Алсыз Лиганд
Күчтүү лиганддар жана алсыз лиганддар - металл ионунун d орбиталдарынын эки энергетикалык деңгээлге бөлүнүшүн шарттаган аниондор же молекулалар. Күчтүү лиганддар менен алсыз лиганддардын ортосундагы айырма күчтүү талаа лигандын байланыштыргандан кийин бөлүнүү жогорку жана төмөнкү энергетикалык деңгээлдеги орбиталдардын ортосунда чоң айырманы пайда кылат, ал эми алсыз талаа лигандын байлагандан кийин орбиталдардын бөлүнүшү жогорку жана төмөнкү ортосундагы айырманы азайтат. энергия деңгээлинин орбиталары.






